Informe por
Recall notice
Lipodrene Suplemento dietético - recordado debido a la presencia de 1,4-dimetilamilamina
hace 4 años •source fda.gov
United States
Nombre de la empresa: Hi-Tech Pharmaceuticals. IncMarca: Hi-Tech Pharmaceuticals. Inc
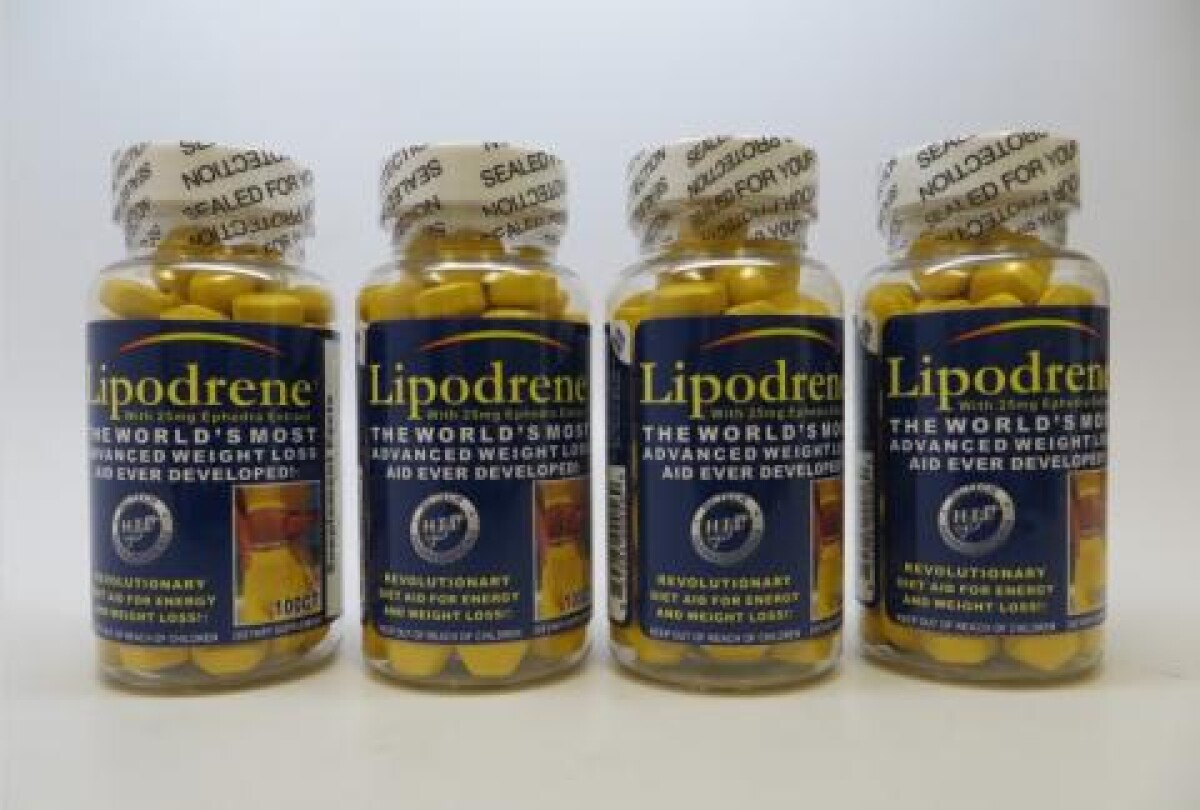
Producto retirado: Lipodrene w/25mg Extracto de Ephedra Suplemento Dietético
Motivo del recuerdo: Presencia de 1,4-dimetilamilamina (DMAA)
Fecha de retirada de la FDA: 12 de mayo de 2021
Recordemos detalles: Productos farmacéuticos de alta tecnología. Inc. de Norcross, GA está recordando el lote # 001211197, Exp. 12/25 de Lipodrene w/25mg Extracto de Ephedra Suplemento Dietético debido a la presencia de 1,4-dimetilamilamina (DMAA). La FDA ha advertido que el DMAA es peligroso porque puede estrechar los vasos sanguíneos y las arterias y causar un aumento correspondiente de la presión arterial u otros problemas cardiovasculares, tales como: dificultad para respirar, arritmias, presión arterial elevada, apriete en el pecho y ataque al corazón. ( www.fda.gov/food/dietary-supplement-products-ingredients/dmaa-products-marketed-dietary-supplements) Hi-Tech Pharmaceuticals, Inc. está llevando a cabo una investigación continua sobre el problema.
Hasta la fecha no se han notificado enfermedades. El retiro voluntario fue el resultado del análisis de la FDA que mostró la presencia de 1,4-dimetilamilamina en un lote de Lipodrene. Se aconseja a los clientes que hayan comprado Lipodrene Lot # 001211197 que dejen de usar este lote de producto inmediatamente y devolverlo al lugar de compra para un reembolso completo. Lipodrene Lote # 001211197 fue comprado y distribuido a través de ventas mayoristas y directas en los Estados Unidos y Puerto Rico, y a través de ventas en línea para uso personal y venta al por menor.
Los minoristas que tengan cualquiera de estos productos deben retirarlos de los estantes y devolverlos a Hi-Tech inmediatamente. Los mayoristas o distribuidores deben alertar a sus clientes sobre la retirada y hacer que devuelvan cualquier producto al lugar de compra o a Hi-Tech Pharmaceuticals. Hi-Tech reemplazará inmediatamente cualquier artículo devuelto por un producto de un lote diferente.
Si tiene alguna pregunta sobre esta retirada, póngase en contacto con Hi-Tech Pharmaceuticals Inc, Norcross, GA al teléfono gratuito 1-888-855-7919 de 9:00am a 5:00pm EST, o puede enviar cualquier solicitud por correo electrónico a recallcoordinator@hitechpharma.com. Su asistencia es apreciada y necesaria para prevenir enfermedades del consumidor.
Este recuerdo se está haciendo con el conocimiento de la Administración de Alimentos y Medicamentos. Las reacciones adversas y los eventos experimentados con el uso de cualquiera de estos productos también deben ser notificados al programa MedWatch de la FDA de Reporting de Eventos Adversos ya sea en línea, por correo ordinario o por fax. www.fda.gov/medwatch/report.htm
Consulta los detalles completos de la retirada en www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/hi-tech-pharmaceuticals-issues-voluntary-recall-lipodrene-w25mg-ephedra-extract-dietary-supplement
Fuente: FDA
312
Comentarios
Comentario