Rapport par
Recall notice
Complément alimentaire au lipodrène - rappel en raison de la présence de 1,4-diméthylamylamine
il y a 4 ans •source fda.gov
United States
Nom de la société : Hi-Tech Pharmaceuticals. IncMarque : Hi-Tech Pharmaceuticals. Inc
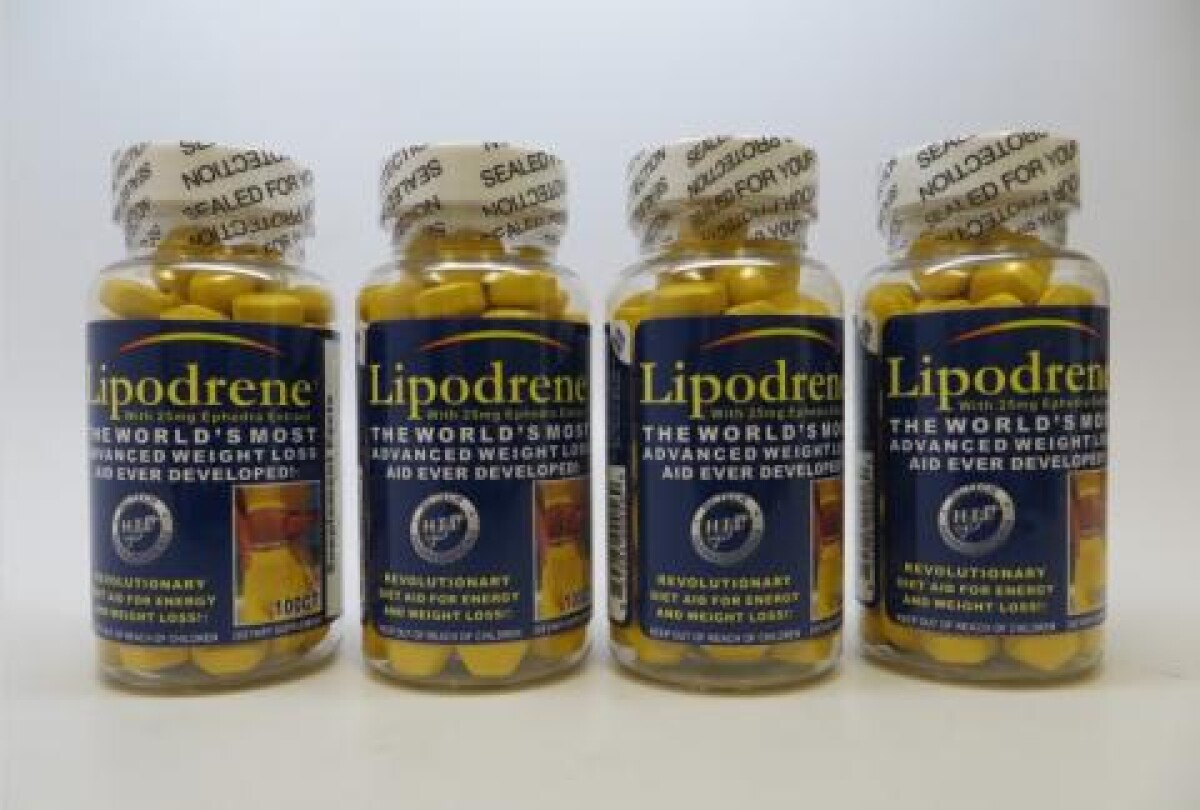
Produit rappelé : Lipodrène w/25 mg Supplément alimentaire à l'extrait d'éphédra
Raison du rappel : Présence de 1,4-diméthylamylamine (DMAA)
Date de rappel de la FDA : 12 mai 2021
Détails du rappel : Produits pharmaceutiques Hi-Tech. Inc. de Norcross, GA rappelle le lot # 001211197, Exp. 12/25 de Lipodrène w/25mg Extrait d'éphédra Supplément alimentaire en raison de la présence de 1,4-diméthylamylamine (DMAA). La FDA a averti que le DMAA est dangereux car il peut rétrécir les vaisseaux sanguins et les artères et provoquer une augmentation correspondante de la pression artérielle ou d'autres problèmes cardiovasculaires, tels que : essoufflement, arythmies, pression artérielle élevée, resserrement de la poitrine, et crise cardiaque. ( www.fda.gov/food/dietary-supplement-products-ingredients/dmaa-products-marketed-dietary-supplements) Hi-Tech Pharmaceuticals, Inc. mène une enquête continue sur le problème.
Aucune maladie n'a été signalée à ce jour. Le rappel volontaire est le résultat d'une analyse de la FDA qui a montré la présence de 1,4-diméthylamylamine dans un lot de lipodrène. Il est conseillé aux clients qui ont acheté Lipodrene Lot # 001211197 de cesser immédiatement d'utiliser ce lot de produit et de le retourner au lieu d'achat pour un remboursement complet. Lipodrene Lot # 001211197 a été acheté et distribué par le biais de ventes en gros et directes aux États-Unis et à Porto Rico, et par le biais de ventes en ligne pour usage personnel et vente au détail.
Les détaillants qui possèdent l'un de ces produits doivent les retirer des rayons et les retourner immédiatement à Hi-Tech. Les grossistes ou les distributeurs devraient avertir leurs clients du rappel et leur demander de retourner tout produit au lieu d'achat ou à Hi-Tech Pharmaceuticals. Hi-Tech remplacera immédiatement tous les articles retournés par des produits provenant d'un lot différent.
Si vous avez des questions au sujet de ce rappel, veuillez communiquer avec Hi-Tech Pharmaceuticals Inc, Norcross, GA, au numéro sans frais 1-888-855-7919 de 9 h à 17 h HNE, ou vous pouvez envoyer une demande par courriel à recallcoordinator@hitechpharma.com. Votre aide est appréciée et nécessaire pour prévenir les maladies du consommateur.
Ce rappel est effectué avec la connaissance de la Food and Drug Administration. Les réactions/événements indésirables observés lors de l'utilisation de ces produits doivent également être signalés au programme MedWatch de la FDA de déclaration des effets indésirables, soit en ligne, par la poste ou par télécopieur. www.fda.gov/medwatch/report.htm
Consultez les détails complets du rappel sur www.fda.gov/safety/recalls-market-withdrawals-safety-alerts/hi-tech-pharmaceuticals-issues-voluntary-recall-lipodrene-w25mg-ephedra-extract-dietary-supplement
Source : FDA
312
Commentaires
Commentaire